일반화학실험 - 어는점내림을 이용한 분자량 측정
일반화학실험 - 어는점내림을 이용한 분자량 측정

일반화학실험 - 어는점내림을 이용한 분자량 측정

Measurement of Freezing Point Depression(어는점내림을 이용한 분자량 측정)
목차
실험 목적
실험원리
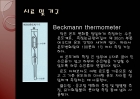
시약 및 기구
실험 방법
실험결과
토의
참고문헌
실험 목적
순수한 용매의 어는점을 이용하여 용액의 어는점을 측정하고, 어는점 내림을 결정하여 비휘발성 물질의 분자량을 결정한다.
실험 원리
총괄성(colligative property)
- 용질의 종류와는 무관하고 오로지 용질 입자의 수에 의해서만 결정되는 성질을 의미
- 1)증기압력 내림, 2)묽은 용액의 삼투압,
3)끓는점 오름, 4)어는점 내림 등 있다.
실험 원리
어는점 내림
-어는점내림을 이용하여 물질의 분자량을 측정하는 방법으로 빙점법 또는 빙점강하법이라고도 한다. 용액의 어는점은 용질의 몰랄농도, 용매의 몰용융열과 분자량 등에 따라 달라진다. 보통 순수한 용매의 어는점은 용질을 가해주면 그 용질의 양에 비례해서 내려간다. 따라서 가해준 용질의 질량을 알고, 용매의 어는점이 내려가는 정도를 측정하면 용질의 분자량을 결정할 수 있다.
실험 원리
어는점 내림 그래프
실험 원리
어는점 내림을 구하는 식
Tf = m x Kf
= 몰랄 어는점 내림 수 (K*kg/mol)
= 순수한 용매의 어는점(T0) 용액의 어는점 (T)
= [R*T0*M1 / 1000*Hf]*m
= 1000*w2*Kf / M2*w1
Tf : 어는점 내림 m : 용질의 몰랄농도 Hf : 용매의 몰용해열
M1 : 용매의 분자량 R : 기체상수 T0 : 순수한 용매의 어는점
Kf : 몰랄 어는점 내림 상수 w1 : 용매의 무게 w2 : 용질의 무게
M2 : 측정하고자 하는 용질의 분자량
M2= Kf*w2*1000 / Tf*w1
실험 원리
....
목차
실험 목적
실험원리
시약 및 기구
실험 방법
실험결과
토의
참고문헌
실험 목적
순수한 용매의 어는점을 이용하여 용액의 어는점을 측정하고, 어는점 내림을 결정하여 비휘발성 물질의 분자량을 결정한다.
실험 원리
총괄성(colligative property)
- 용질의 종류와는 무관하고 오로지 용질 입자의 수에 의해서만 결정되는 성질을 의미
- 1)증기압력 내림, 2)묽은 용액의 삼투압,
3)끓는점 오름, 4)어는점 내림 등 있다.
실험 원리
어는점 내림
-어는점내림을 이용하여 물질의 분자량을 측정하는 방법으로 빙점법 또는 빙점강하법이라고도 한다. 용액의 어는점은 용질의 몰랄농도, 용매의 몰용융열과 분자량 등에 따라 달라진다. 보통 순수한 용매의 어는점은 용질을 가해주면 그 용질의 양에 비례해서 내려간다. 따라서 가해준 용질의 질량을 알고, 용매의 어는점이 내려가는 정도를 측정하면 용질의 분자량을 결정할 수 있다.
실험 원리
어는점 내림 그래프
실험 원리
어는점 내림을 구하는 식
Tf = m x Kf
= 몰랄 어는점 내림 수 (K*kg/mol)
= 순수한 용매의 어는점(T0) 용액의 어는점 (T)
= [R*T0*M1 / 1000*Hf]*m
= 1000*w2*Kf / M2*w1
Tf : 어는점 내림 m : 용질의 몰랄농도 Hf : 용매의 몰용해열
M1 : 용매의 분자량 R : 기체상수 T0 : 순수한 용매의 어는점
Kf : 몰랄 어는점 내림 상수 w1 : 용매의 무게 w2 : 용질의 무게
M2 : 측정하고자 하는 용질의 분자량
M2= Kf*w2*1000 / Tf*w1
실험 원리
....

-
 일반화학실험 - 어는점 내림과 분자량 측정
일반화학실험 - 어는점 내림과 분자량 측정
♠ 실험제목 : 어는점 내림과 분자량 측정 ♠ 실험목적 : 이 실험에서는 용액의 어는점 내림을 이용하여 용질의 분자량을 결정한다 ♠ 실험이론 : 액체의 어는점은 고체와 액체가 평형 상태에 있는 온도이다. 순수.. -
 물리화학실험 - 어는점내림을 이용한 분자량 측정
물리화학실험 - 어는점내림을 이용한 분자량 측정
Measurement of Freezing Point Depression(어는점내림을 이용한 분자량 측정) 목차 실험 목적 실험원리 시약 및 기구 실험 방법 실험결과 토의 참고문헌 실험 목적 순수한 용매의 어는점을 이용하여 용.. -
 일반화학실험 - 어는점 내림법에 의한 분자량 측정
일반화학실험 - 어는점 내림법에 의한 분자량 측정
실험 제목 어는점 내림법에 의한 분자량 측정 실험 목적 이 실험의 목적은 어는점 내림법에 의하여 용질의 분자량을 측정하는 방법을 배우는 데 있다. 실험 이론 ★ 물리화학 실험 내용 ★1) 용질을 가했을 때 용.. -
 [일반화학실험]어는점 내림과 분자량
[일반화학실험]어는점 내림과 분자량
어는점 내림과 분자량 1. 실험 제목 -어는점 내림과 분자량 2. 실험 목적 -어는점 내림을 이용하여 분자량을 결정하고 용액의 총괄성과 라울의 법칙을 이해한다. 3. 실험 방법 1)Hot plate에 250 mL 비커를 이.. -
 [화학실험] 어는점 내림에 의한 분자량 측정
[화학실험] 어는점 내림에 의한 분자량 측정
[화학실험] 어는점 내림에 의한 분자량 측정 1. 실험목적 비극성 용매인 벤젠을 이용하여, 벤젠에 어는점이 다른 용질을 넣었을 때 얼마나 내려가는지를 측정하고 이로부터 용질의 분자량을 구할 수 있다. 2. 실.. -
 물리화학 실험 - 어는점 내림에 의한 분자량 측정
물리화학 실험 - 어는점 내림에 의한 분자량 측정
실험. 어는점 내림에 의한 분자량 측정 실 험 목 적 ① 어는점 내림 현상을 이해하고 이를 이용하여 용질의 분자량을 결정한다. ② Raoult의 법칙, 총괄성의 개념을 이해한다. 원리 및 이해 (1) Raoult의 법칙 .. -
 일반화학 실험보고서 - Ascorbic acid의 분자량 결정
일반화학 실험보고서 - Ascorbic acid의 분자량 결정
일반화학 실험보고서 - Ascorbic acid의 분자량 결정 1. Abstract 이 실험에서는 저번 시간과 마찬가지로 어떤 물질의 분자량을 구하는 것이 목적이다. 지난번에 이산화탄소의 분자량을 구할 때는 이상기체 상.. -
 일반화학 실험보고서 - Ascorbic acid의 분자량 결정
일반화학 실험보고서 - Ascorbic acid의 분자량 결정
일반화학 실험보고서 - Ascorbic acid의 분자량 결정 1. Abstract 이 실험에서는 저번 시간과 마찬가지로 어떤 물질의 분자량을 구하는 것이 목적이다. 지난번에 이산화탄소의 분자량을 구할 때는 이상기체 상.. -
 비타민C[Ascorbic acid]의 분자량 결정
비타민C[Ascorbic acid]의 분자량 결정
일반화학 실험보고서 Ascorbic acid의 분자량 결정 1. Abstract 이 실험에서는 저번 시간과 마찬가지로 어떤 물질의 분자량을 구하는 것이 목적이다. 지난번에 이산화탄소의 분자량을 구할 때는 이상기체 상태.. -
 물리화학실험 - 어는점 내림법에 의한 분자량 측정
물리화학실험 - 어는점 내림법에 의한 분자량 측정
실험 제목 어는점 내림법에 의한 분자량 측정 실험 목적 이 실험의 목적은 어는점 내림법에 의하여 용질의 분자량을 측정하는 방법을 배우는 데 있다. 실험 이론 ★ 물리화학 실험 내용 ★1) 용질을 가했을 때 용..